Глава VIII: План Сотворения Необходимых Для Жизни Элементов
Глава VIII: План Сотворения Необходимых Для Жизни Элементов
В основе Вселенной лежат разум и воля. В том, как абстрактная математика проникает в секреты Вселенной, есть знак этого божественного присутствия, разума, сотворившего мир. Природа идеально настроена на то, чтобы дать возможность возникнуть жизни и сознанию. Джон Полкингхорн, английский физик 84
До сих пор мы рассматривали физическое равновесие мира, созданное с таким расчетом, чтобы мы могли жить в нем. Мы увидели, как совершенен замысел структуры Вселенной, расположение Земли, ее воздуха, света и воды, которым приданы все необходимые для жизни свойства. Если посмотреть на химические элементы – строительный материал для наших рук, глаз, волос и органов, а также всех живых существ: растений и животных, которые являются источниками нашей пищи, то мы увидим, что они созданы так, чтобы служить той цели, которой они поставлены служить.
 |
Физик Роберт Е. Д. Кларк так говорит об особом божественном плане создания строительных материалов жизни: «Возникает впечатление, что Создатель дал нам набор сборных конструкций, готовых для предстоящей работы» 85 .
Самым важным строительным материалом является углерод.
План Создания Углерода
В предыдущих главах мы рассказывали о необыкновенном процессе, в результате которого в самом сердце гигантских звезд под названием «красные гиганты» образуется углерод, шестой элемент периодической системы. Мы также упоминали о том, как Фред Хойл, потрясенный открытием этого удивительного процесса, сказал, что «законы ядерной физики были созданы с учетом тех последствий, которые они вызывают внутри звезд» 86 .
Действительно, не только физическое строение этого элемента, но и его химические свойства были созданы такими, какими им надлежит быть.
Чистый углерод встречается в природе в виде графита и алмаза. Однако он входит в состав компонентов других элементов, создавая различные вещества. Так, мембрана клетки и кора дерева, хрусталик глаза и рог оленя, белок яйца и яд змеи – весь этот разнообразный органический материал создан на основе углеродсодержащих

Karbon atomu doğada genellikle grafit halinde bulunur. Ancak bu kara madde, diğer atomlarla birleştiğinde ortaya olağanüstü derecede farklı maddeler çıkarır. Canlı bedenlerini oluşturan malzeme, karbonun diğer birkaç element ile kurduğu bu bağlardır.
компонентов. В соединении с водородом, кислородом и азотом в различных количествах и геометрических формах углерод дает огромный ассортимент материалов с самыми разными свойствами.
Некоторые молекулы углеродных соединений состоят всего лишь из нескольких атомов, другие – из тысяч и даже миллионов. Более того, все другие элементы уступают углероду в прочности и стабильности создания молекул. В книге «Жизнь» Дейвид Берни отмечает: «Углерод – очень необычный элемент. Без углерода и его необыкновенных свойств маловероятно, что на Земле зародилась бы жизнь» 87 .
«В ряду других элементов углерод уникален по количеству и разнообразию создаваемых соединений», – пишет английский физик Невил Сиджвик в работе «Химические элементы и соединения». Далее он говорит: «Уже выделено и описано около четверти миллиона, но и это дает весьма несовершенную картину его возможностей, поскольку углерод является основой всех форм живой материи» 88 .
С точки зрения физики и химии жизнь не может быть основана ни на каком другом элементе, кроме углерода. Одно время считалось, что кремний может быть еще одним элементом, на котором могла бы основываться жизнь. Теперь мы знаем, что такое предположение ошибочно. Еще раз процитируем Сиджвика: «Мы уже достаточно знаем сейчас, чтобы с уверенностью сказать – мир, в котором кремний занял бы место углерода как основы жизни, невозможен…» 89 .
Ковалентные Связи
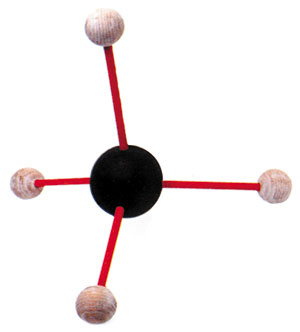 |
| Metan gazının yapısı: Ortadaki karbon atomunun etrafına dört ayrı hidrojen atomu bağlı. |
Химические связи, в которые вступает углерод, образуя органические соединения, называются «ковалентными связями». Считается, что ковалентная связь устанавливается, когда два атома имеют общие электроны.
Электроны атома образуют особые оболочки, располагающиеся вокруг ядра. Внутренняя оболочка не может иметь больше двух электронов, в следующей оболочке может быть не более восьми электронов. В третьей – их число может доходить до восемнадцати. Число электронов увеличивается с каждой следующей оболочкой. В этой схеме интересно то, что атом, кажется, стремится укомплектовать число электронов в каждой оболочке. Водород, например, имеет шесть электронов во второй (самой удаленной) оболочке, поэтому он готов вступать в соединения с другими атомами, которые дадут ему еще два электрона, чтобы увеличить их количество до восьми. (Почему атомы ведут себя таким образом, до сих пор неизвестно, но то, что они так поступают, очень хорошо, поскольку, если бы они этого не делали, не было бы жизни.)
Ковалентные связи – результат стремления атомов пополнить свои электронные оболочки. Два или более атомов могут восполнить недостаток электронов, поделившись ими друг с другом. Хороший пример – молекула воды (Н2О), строительный материал которой (два атома водорода и один атом кислорода) создает ковалентную связь. В этом соединении кислород доводит число электронов второй оболочки до восьми за счет двух электронов оболочек (по одному от каждого) двух атомов водорода. Точно так же атомы водорода «берут в долг» один электрон кислорода, чтобы пополнить свои собственные оболочки.
Углерод легко создает ковалентные связи с другими атомами (включая атомы углерода), на основе которых может возникать огромное число разнообразных соединений. Одно из самых простых соединений – метан, обычный газ, создаваемый ковалентной связью четырех атомов водорода и одного атома углерода. Углерод имеет только шесть электронов во внешней оболочке, и ему не хватает четырех электронов, а не двух, как в случае с кислородом; поэтому, чтобы обеспечить требуемое количество электронов, необходимы четыре атома водорода.
Исключительная способность углерода образовывать связи с другими атомами уже отмечалась нами. Класс соединений, состоящих исключительно из углерода и водорода, называется углеводородами. Это огромная семья соединений, включающая природный газ, жидкую нефть, керосин и смазочные масла. Такие углеводороды, как этилен и пропилен, представляют собой основу современной нефтехимической промышленности. Бензол, толуол и живица – углеводороды, знакомые всем, кто когда-либо работал с красками. Нафталин, защищающий нашу одежду от моли, – еще один углеводород. При добавлении хлора или фтора некоторые углеводороды приобретают функции анестезирующих веществ, кроме того, они образуют вещества, используемые в огнетушении или же фреон – газ, широко используемый при замораживании.
 |
| Zeytinyağı, et ya da şeker gibi farklı maddeler, karbon, hidrojen, oksijen ya da azot atomlarının farklı tasarımlarda birleşmeleriyle oluşur. |
Существует еще один класс соединений с углеродом, водородом и кислородом на основе ковалентной связи. В этой группе мы находим спирты, такие как этанол, пропанол, кетоны, альдегиды, жирные кислоты и многие, многие другие вещества. Еще одну группу соединений углерода, водорода и кислорода составляет сахар, включая глюкозу и фруктозу.
Целлюлоза, составляющая основу дерева и сырья для бумаги, уксус, пчелиный воск и муравьиная кислота – это также углеводороды. Каждое соединение из невероятно богатого арсенала веществ и материалов, встречающихся в природе, есть не что иное, как различные сочетания углерода, водорода и кислорода, соединенных ковалентной связью.
Su ve Metan: Kovalent Bağlarin İki Farkli Örneği |
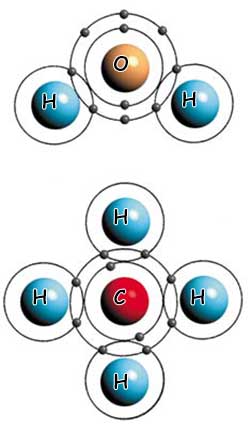 |
| Üstteki su molekülü, iki hidrojen ve bir oksijen atomu arasındaki kovalent bağla kurulmuştur. Alttaki metan molekülü ise, dört hidrojen atomunun bir karbon atomu ile kovalent bağ yapmasıyla oluşmuştur. |
Когда углерод, водород и азот вступают в такие связи, в результате возникают молекулы, составляющие основу и структуру самой жизни, – аминокислоты, которые образуют белки. Нуклеотиды, участвующие в построении ДНК, – это тоже молекулы, созданные из углерода, водорода, кислорода и азота.
Иными словами, ковалентные связи, в которые может вступать атом углерода, оказываются жизненно важными. Если бы углерод, водород, азот и кислород не стремились с такой готовностью делиться электронами друг с другом, жизнь была бы невозможна.
Столь важную для существования жизни способность углерода вступать в такие связи химики называют «метастабильностью». Биохимик Дж. В. С. Халдейн определяет метастабильность следующим образом:
метастабильная молекула – это молекула, которая высвобождает энергию путем трансформации, но она достаточно стабильна, чтобы существовать длительное время, если не будет активирована при помощи тепла, излучения или соединения с каким-либо катализатором 90 . Из этого довольно технического определения следует, что углерод обладает уникальной структурой, благодаря которой при нормальных условиях он с большой легкостью устанавливает ковалентные связи.
Но именно здесь положение дел становится особенно любопытным, поскольку углерод метастабилен только в очень узком диапазоне температур. При температуре выше 100оС соединения углерода становятся нестабильными.
Это настолько хорошо известный факт, что многие его даже не замечают. Например, когда мы жарим мясо, мы изменяем структуру его углеродных соединений.
Приготовленное мясо становится абсолютно «мертвым», т.е. его химическая структура отлична от той, какая у него была, когда оно было частью живого организма. В самом деле, большинство соединений углерода теряют свойства живой материи при температуре свыше 100оС: распадается большинство витаминов, сахара претерпевают структурные изменения и, теряют питательные свойства. При температуре 150оС углеродные соединения начинают гореть.
Иными словами, для того, чтобы соединения углерода оставались неизменными, окружающая температура не должна превышать 100оС. Нижний предел – 0оС, если температура упадет намного ниже 0оС, органическая биохимия станет невозможной.
В случае других соединений это не так. Большинство неорганических соединений не метастабильны, т.е. их стабильность не зависит в такой степени от колебаний температуры. Чтобы убедиться в этом, давайте проведем эксперимент. Насадите кусок мяса на железный шампур и положите его над огнем. Когда температура повысится, мясо станет коричневым и в конце концов сгорит, а железному шампуру ничего не сделается. То же самое произойдет, если заменить железо камнем или стеклом. Пришлось бы очень сильно увеличить температуру, чтобы структура этих материалов начала меняться.
К этому моменту вы, наверное, уже поняли, что диапазоны температур, необходимых для того, чтобы ковалентные связи углеродных соединений установились и остались постоянными, сходен с температурами, существующими на нашей планете. Мы говорили ранее, что диапазон температур во Вселенной огромен – от миллионов градусов в недрах звезд до абсолютного нуля (-273,15оС). Узкий диапазон температурных колебаний на Земле, сотворенной для человека, обеспечивает возможность создания углеродных соединений – строительного материала жизни.
Но на этом любопытные «совпадения» не заканчиваются. Только при такой температуре вода остается жидкой, а жидкая вода, как мы знаем, – одно из основных требований жизни.
Следовательно, для того, чтобы вода оставалась жидкой, а соединения углерода - постоянными, необходим один и тот же температурный режим. Такой режим и предоставляется им на планете Земля. Нет никаких физических или естественных законов, устанавливающих такое положение дел. Но эта ситуация – еще одно свидетельство того, что вода, углерод и сама Земля сотворены так, чтобы находиться в абсолютной гармонии друг с другом.
Слабые Связи
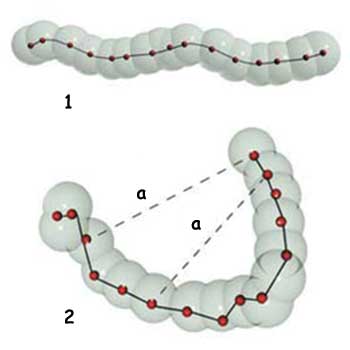 |
| a. Zayıf bağ 1. Kovalent bağ: Atomlar birbirleri ile sıkı sıkıya tutturulmuş. 2. Zayıf bağ: Atom zinciri farklı noktalardan birbirine üç boyutta tutturulmuş |
Наряду с ковалентными связями существует еще один, совершенно отличный тип связи, известный как слабые связи.
Эти связи приблизительно в двадцать раз слабее ковалентных, отсюда их название, но они не менее важны для существования процессов органической химии. Именно благодаря слабым связям белки – строительный материал всех живых организмов – способны сохранять свою сложную и жизненно важную трехмерную структуру.
Чтобы объяснить суть этого процесса, необходимо дать краткие сведения о структуре белка. Белки часто называют «цепочкой» аминокислот. Хотя эта метафора правильна по сути, она не совсем верно отражает ситуацию. Большинство людей представляет «цепочку» аминокислот в виде бус из жемчуга, в то время как составляющие белок аминокислоты имеют трехмерную структуру и больше похожи на ветвистое дерево.
Ковалентные связи объединяют аминокислоты, а слабые – поддерживают трехмерную структуру этих кислот. Ни один белок не может существовать без слабых связей, а без белка не было бы жизни.
Физическая и химическая природа ковалентных и слабых связей различна, и они абсолютно не зависят друг от друга. Тем не менее, оба типа связей могут формироваться и оставаться постоянными только в одном и том же очень узком температурном диапазоне, точно совпадающем с земным.
Майкл Дентон в книге «Предназначение природы» подчеркивает это удивительное соответствие фундаментальных основ жизни:
«В огромном диапазоне космических температур существует только один маленький участок, в котором мы имеем: 1. жидкую воду, 2. огромное количество метастабильных органических соединений и 3. слабые связи, делающие устойчивой трехмерную структуру сложных молекул» 91 .
Из всех небесных тел такой «узкий температурный участок» существует только на Земле. Более того, именно на Земле два основных строительных материала – углерод и вода – обнаруживаются в достаточном количестве.
Не свидетельствует ли это о том, что атом углерода с его необыкновенными свойствами и наша планета были сотворены для того, чтобы Земля стала нашим домом?
План Сотворения Кислорода
Итак, мы знаем теперь, почему углерод является основой строения всех живых организмов, и что он был сотворен таким образом, чтобы выполнять предназначенную ему функцию. Однако существование углеродных форм жизни зависит еще от одного фактора – энергии. Энергия – необходимое требование жизни.
Зеленые растения получают энергию от Солнца в ходе фотосинтеза. Для всех остальных живых организмов, включая человека, единственный источник энергии – процесс «окисления» или «горения». Энергия дышащих кислородом организмов образуется в результате сжигания питания, поступающего от растений и животных. Термин «окисление» употребляется для обозначения химической реакции, в ходе которой вещества окисляются, или, иначе говоря, сгорают, соединяясь с кислородом. Вот почему кислород столь же необходим, как углерод и водород.
Обобщенная формула горения (окисления) выглядит следующим образом: соединение углерода + кислород > вода + углекислый газ + энергия. Из формулы следует, что соединения углерода и кислорода, объединяясь (естественно, при определенных условиях) друг с другом, образуют воду и углекислый газ, а также значительное количество энергии. Наиболее активно эта реакция протекает в углеводородах (соединение водорода и углерода). Глюкоза (сахар и углеводороды) постоянно сжигается в нашем теле, чтобы обеспечить его необходимым количеством энергии.
В этапах этого сложного процесса мы находим необыкновенную гармонию: углеводороды наиболее приспособлены для участия в реакции окисления, водород с готовностью соединяется с кислородом, создавая большое количество энергии. При этом для сжигания в кислороде невозможно найти лучшего топлива, чем водород, углерод стоит на третьем месте после водорода и бора. Лоуренс Хендерсон в книге «Гармония окружающей среды» пишет об этом так:
«Химические превращения по многим причинам наиболее приспособлены для того, чтобы стать физиологическими процессами, т.е. теми процессами, которые заставляют огромный поток энергии вливаться в реку жизни» 92 .
План Сотворения Огня, Или Почему Мы Не Сгораем
 |
Как мы только что видели, окисление углеводородов представляет собой фундаментальную реакцию, которая высвобождает энергию, необходимую для жизни организмов, дышащих кислородом. Но этот простой факт вызывает у нас некоторое беспокойство. Если наши тела в основном состоят из углеводородов, почему они не окисляются? Иначе говоря, почему мы не воспламеняемся, как зажженная спичка?
Тело человека находится в постоянном соприкосновении с кислородом воздуха, и все-таки оно не окисляется и, следовательно, не загорается. Почему?
Причина этого парадоксального явления состоит в том, что при обычных показателях температуры и давления молекулярная форма кислорода (О2) имеет значительную степень инертности, т.е. она не способна вступать в реакцию с другими веществами. Но здесь возникает другой вопрос: если молекула кислорода настолько инертна, что не стремится превратить нас в пепел, что заставляет ту же самую молекулу вступать в химические реакции внутри нашего тела?
Ответ на этот вопрос, над решением которого химики бились еще в середине XIX века, был найден только во второй половине XX столетия, когда были открыты ферменты. Функция ферментов состоит в том, что они побуждают молекулярную форму кислорода атмосферы вступать в химические реакции. В процессе серии сложных превращений в организме человека ферменты используют атомы железа и меди в качестве катализаторов. Катализатор – это вещество, инициирующее химическую реакцию и обеспечивающее ее протекание в условиях, в которых она невозможна, например, при понижении температуры 93 .
В данном случае мы имеем очень интересную ситуацию: кислород способствует окислению и горению, и, логически рассуждая, он должен был бы сжигать и нас. Чтобы избежать этого, молекулярной форме кислорода (О2), существующей в атмосфере, было придано качество химической инертности, т.е. неспособности легко вступать в реакции. С другой стороны, человеческий организм зависит от энергии, возникающей в результате окислительных свойств кислорода, поэтому его клетки были снабжены чрезвычайно сложной ферментной системой, которая активирует этот инертный газ.
Ферментная система – прекрасный пример божественного плана, и никакая эволюционная теория, утверждающая, что жизнь есть результат случайности, не в состоянии объяснить ее 94 .
Свойство, которое английский химик Невил Сиджвик называет «специфической инертностью углерода» 95 , – еще одна мера предосторожности, необходимая для защиты наших тел от возгорания. Это означает, что углерод при обычных показателях давления и температуры не стремится вступать в реакцию с кислородом. Это может показаться непонятным. Однако каждый, кому приходилось разжигать огонь в полном толстых поленьев очаге зимой или для шашлыка летом, хорошо знает, что для того, чтобы огонь загорелся, необходимо положить в него растопку или поднести к топливу факел. Но как только огонь начинает гореть, углерод быстро вступает в реакцию с кислородом и высвобождает большое количество энергии. Вот почему так трудно разжечь огонь без дополнительного источника тепла. После возгорания образующееся тепло побуждает соединения углерода загораться, и огонь начинает распространяться.
И снова мы видим, что огонь представляет собой очень интересный пример общего плана. Химические свойства кислорода и углерода устроены таким образом, чтобы эти два элемента вступали в реакцию друг с другом только при наличии большого количества тепла. Если бы кислород и углерод были чуть более активными в их стремлении соединиться друг с другом, это приводило бы к самовоспламенению. При чуть более жаркой погоде спонтанное возгорание людей, деревьев и животных было бы обычным явлением. Идущий в пустыне путник в полдень, когда особенно жарко, мог бы внезапно загореться, то же самое могло случиться с растениями и животными. Если бы в таком мире жизнь и существовала, в ней было бы мало радости.
С другой стороны, если бы углерод и кислород были немного более инертны (т.е. менее реактивны), было бы очень трудно, а может быть и невозможно, разжечь огонь в этом мире. А без огня мы были бы не в состоянии согреться. Вполне вероятно, не было бы никакого технического прогресса на нашей планете, поскольку прогресс предполагает производство таких материалов, как металл, а без тепла, которое дает нам огонь, производство металлов невозможно.
Все это показывает, что химические свойства углерода и водорода спланированы так, чтобы наилучшим образом служить человеку. Майкл Дентон пишет: «Удивительная инертность атомов углерода и кислорода при окружающих температурах, сопряженная с огромными энергиями, возникающими при их соединении, имеет большое значение для жизни на Земле. Это странное сочетание не только дает возможность высшим формам жизни получать огромное количество энергии в процессе контролируемых и упорядоченных реакций, но и позволяет человеку использовать и обуздать огромную энергию горения и направить ее на развитие техники» 96 .
Другими словами, свойства углерода и кислорода были сотворены с таким расчетом, чтобы они наиболее соответствовали потребностям жизни человека. Эти свойства дают нам возможность развести огонь и пользоваться им так, как нам удобно. Более того, наш мир полон вещей, легко горящих (например, древесина) и поставляющих нам углерод. Все это указывает на то, что огонь и материалы для разжигания и поддерживания его были созданы для жизни. В Коране Господь обращается к людям с такими словами:
«Он - Тот, Кто создал вам огонь из дерева живого, и от него вы зажигаете свои огни» (Коран, 36:80).
Идеальная Растворимость Кислорода
Использование кислорода организмом в большой степени зависит от свойства этого газа растворяться в воде. Кислород, который мы вдыхаем, сразу же растворяется в крови. Гемоглобин, один из видов белка, поглощает молекулы кислорода и переносит их в другие клетки, где благодаря ферментной системе кислород используется для окисления соединения углерода – АТФ, в результате чего высвобождается энергия.
Все сложные организмы получают энергию подобным образом, однако работа этой системы зависит от растворимости кислорода.
Если бы кислород обладал меньшей растворимостью, в кровеносную систему поступало бы недостаточно кислорода, и клетки были бы неспособны производить необходимую им энергию. С другой стороны, если бы растворимость кислорода была слишком большой, в крови образовался бы избыток кислорода, что привело бы к кислородному отравлению.
Диапазон показателей растворимости газов в воде огромен, самый растворимый газ в миллион раз более растворим в воде, чем газ с наименьшей растворимостью. Вряд ли существуют какие-нибудь газы с идентичными показателями растворимости. Растворимость углекислого газа в воде в двадцать раз больше, чем у кислорода. В этом огромном диапазоне показателей растворимость, которой обладает кислород, оказывается точно такой, какая требуется для существования жизни.
Что бы произошло, если бы показатель растворимости кислорода в воде был другим: чуть больше или чуть меньше? В случае если растворимость меньше, в кровь поступает меньше кислорода, и у клеток возникает кислородное голодание. Такое положение дел значительно затруднило бы жизнь организмов с активными метаболическими процессами обмена, таких как человек. Как бы вы ни старались глубоко и часто дышать, вы бы постоянно задыхались, потому что клетки не получали бы необходимого количества кислорода.
Если бы растворимость кислорода в воде была больше, вам бы грозила опасность кислородного отравления, о котором мы говорили выше. Кислород – довольно опасное вещество: если организм получает его слишком много, может наступить смерть. Часть кислорода в крови вступает в химическую реакцию с водой крови, и, если количество растворенного кислорода слишком велико, образуются очень активные и опасные побочные продукты. Одна из функций сложной ферментной системы крови состоит в том, чтобы не допустить этого. Однако при значительном повышении количества растворенного в крови кислорода система может не справиться с работой, в результате с каждым вдохом будет нарастать общее отравление организма и наступит смерть. По словам химика Ирвина Фридовича,
«все дышащие организмы находятся в большой опасности. Тот самый кислород, который поддерживает их жизнь, на самом деле вреден им, но они странным образом выживают. Это происходит вследствие действия сложной структуры защитных механизмов» 97 .
От отравления избытком кислорода нас спасает то, что растворимость кислорода и сложная ферментная система человеческого организма созданы так, как нужно, и в необходимом соответствии друг с другом. Аллах сотворил воздух, которым мы дышим, и все системы, чтобы пользоваться ими наилучшим образом, и установил совершенную гармонию между ними.
Другие Элементы
 |
| Bakır |
Углерод и кислород – не единственные элементы, созданные для поддержания жизни. Водород и азот, составляющие значительную часть живых организмов, также обладают жизненно важными свойствами. Фактически нет ни одного элемента в периодической системе, который не выполнял бы ту или иную функцию поддержания жизни.
В периодической системе девяносто два элемента, самый легкий из которых водород, а самый тяжелый – уран. (Кроме урана есть и другие тяжелые элементы, но они не встречаются в естественных условиях, а были созданы только в лабораториях, к тому же все они очень неустойчивы.) Из девяноста двух элементов только двадцать пять непосредственно необходимы для жизни, и только одиннадцать из них – водород, углерод, кислород, азот, натрий, магний, фосфор, сера, хлор, калий и кальций – составляют 99% веса тела почти всех живых организмов. Остальные 14% – ванадий, хром, марганец, железо, кобальт, никель, медь, цинк, молибден, бром, кремний, селен, фтор и йод – присутствуют в живых организмах в очень малых количествах, но и они выполняют важные жизненные функции. Три элемента – мышьяк, олово и вольфрам – обнаруживаются только в некоторых живых организмах, и их действие еще не полностью раскрыто. Еще три элемента – бром, стронций и барий – присутствуют в большинстве организмов, но какую функцию они выполняют, до сих пор остается загадкой 98 .
 |
| Magnezyum |
Все элементы периодической системы тем или иным образом участвуют в поддержании жизни. Это подтверждают Р. Фаусто де Сильва и Р. Дж. П. Вильямс в книге «Биологическая химия элементов»: «Кажется, биологические элементы были выбраны практически из всех групп и подгрупп периодической таблицы... И это значит, что почти все виды химических свойств связаны с жизненными процессами в рамках, ограниченных условиями окружающей среды» 99 .
Даже радиоактивные элементы в самом конце периодической таблицы были задействованы, чтобы служить жизни человека. В книге «Предназначение природы» Майкл Дентон подробно описывает важную роль таких радиоактивных элементов, как уран, в создании геологической структуры Земли. Возникающая естественным образом радиоактивность обеспечивает способность земного ядра сохранять свое тепло. Жидкое ядро, состоящее из железа и никеля, – источник магнитного поля Земли, которое, выполняя самые различные функции, защищает планету от опасного излучения и космических частиц. Даже инертные газы и редкоземельные металлы, хотя и не вовлечены в процесс поддержания жизни, существуют для обеспечения необходимого набора присутствующих в естественной среде элементов, вплоть до урана 100 .
Как мы видели, все известные элементы земли служат человеку. Каждый из них нужен и имеет определенное значение. Это является еще одним доказательством того, что Аллах сотворил мир для человека.
 |
Заключение
Все физические и химические свойства Вселенной таковы, какими они должны быть, чтобы существовала жизнь. В этой книге мы лишь заглянули в хранилище данных, подтверждающих этот факт. Однако, даже если бы мы зашли в него и подробно изучили его содержимое, этот факт остался бы неизменным. В каждой детали Вселенной, столь совершенно замысленной и упорядоченной, присутствует одна цель: сделать жизнь человека возможной.
В этом есть доказательство существования Создателя, сотворившего Вселенную для этой цели. Все свойства материи несут в себе Бесконечное знание, Мудрость и Силу Аллаха, который сотворил Вселенную из ничего. Все склоняется перед Его волей, и каждая отдельная деталь находится в совершенной гармонии со всем остальным.
Эта истина, которую, наконец, признала научная мысль ХХ века, была открыта человечеству в Коране 14 столетий назад – Аллах сотворил каждую деталь Вселенной, чтобы раскрыть совершенство Его творения:
«Благословен будь Тот, в руках Которого вся власть над миром, Кто Всемогущ над всем и вся! Кто создал смерть и жизнь, чтоб испытать, кто праведней из вас в своих деяньях. Велик в Могуществе Своем, и отдающ во всепрощенье Он! Он – Тот, Кто создал семь небес рядами. В Божественном творенье том не различить тебе структурных нарушений. И снова обратив свой взор, - ты зришь какой-нибудь изъян в творенье этом? И вновь свой взор ты обрати: вернется он униженным и тщетным» (Коран, 67:1-4).
Источники
84. "Science Finds God", Newsweek, 27 Temmuz 1998
85. Robert E. D. Clark, The Universe: Plan or Accident?, London, Paternoster Press, 1961, s. 98
86. Fred Hoyle, Religion and the Scientists, London: SCM, 1959; M. A. Corey, The Natural History of Creation, Maryland: University Press of America, 1995, s. 341
87. David Burnie, Life, Eyewitess Science, London: Dorling Kindersley, 1996, s. 8
88. Nevil V. Sidgwick, The Chemical Elements and Their Compounds, vol 1. Oxford: Oxford University Press, 1950, s. 490
89. Nevil V. Sidgwick, The Chemical Elements and Their Compounds, vol 1., s. 490
90. J. B. S. Haldane, "The Origin of Life", New Biology, 1954, vol. 16, s. 12
91. Michael Denton, Nature's Destiny, s. 115-116
92. Lawrence Henderson, The Fitness of the Environment, Boston: Beacon Press, 1958, s. 247-48
93. L. L. Ingraham, "Enzymic Activation of Oxygen", Comprehensive Biochemistry, (ed. M. Florkin, E. H. Stotz), Amsterdam: Elsevier, vol. 14, s. 424
94. Происхождение сложнейшей энзимной системы организма, обеспечивающей кислородное дыхание, является одним из множества вопросов, на которые теория эволюции не может дать хоть какого-либо объяснения. Особенность данной энзимной системы такова, что она может функционировать только в самом полном и совершенном виде, она будет полностью непригодна при отсутствии даже самого малозаметного звена. Таким образом, эту систему невозможно разложить на упрощенные составляющие. Следовательно, в данном случае нельзя говорить об эволюции жизни на Земле от простого к сложному, как это утверждают дарвинисты. Один из самых ярых сторонников теории эволюции в Турции, профессор биологии Университета Хаджеттепе Али Демирсой сделал такое признание относительно этой проблемы:
«Однако в данной ситуации присутствует один неразрешимый момент. Митохондрии используют определенное количество энзимов (ферментов) для дробления кислорода. Отсутствие хотя бы одного из данных энзимов приведет к полной остановке всей системы преобразования кислорода. Кроме того, преобразование кислорода в энергию не может быть постепенным, поэтапным процессом. Похоже, что эти процессы возможны только в совершенной системе. Поэтому, в данном случае мы вынуждены отказаться от теории поэтапного развития, которую мы отстаивали до сих пор. Похоже, что все энзимы (энзимы Кребса), необходимые митохондриям для преобразования кислорода в энергию, как бы ни была мала вероятность этого предположения, произошли одновременно, они либо попали внутрь клетки сразу в совершенном виде, либо же возникли внутри клетки, но также одновременно и в своем окончательном виде. Ибо все системы, которые не могли использовать кислород в полной мере, то есть промежуточные системы, должны были бы исчезнуть при первом же контакте с кислородом.
( Ali Demirsoy, Yaşamın Temel Kuralları: Genel Biolojı, Genel Zoolojı, cilt 1, kısım 1, Ankara,1998, s.578)
Вероятность случайного возникновения одного лишь энзима (особого белка) из тех, о которых профессор Али Демирсой сказал «мы вынуждены признать, что все они возникли случайно и одномоментно», равна 1 к 10950, а это абсолютно недопустимая вероятность в математике. Таким образом, заявления эволюционистов о возможности случайного возникновения всех энзимов сразу, противоречит элементарной логике и здравому смыслу.
95. Nevil V. Sidgwick, The Chemical Elements and Their Compounds, vol 1. Oxford: Oxford University Press, 1950, s. 490
96. Michael Denton, Nature's Destiny, s. 122-123
97. Irwin Fridovich, "Oxygen Radicals, Hydrogen Peroxide, and Oxygen Toxicity", Free Radicals in Biology, (ed. W. A. Pryor), New York: Academic Press, 1976, s. 239-240
98. J. J. R. Fraústo da Silva, R. J. P. Williams, The Biological Chemistry of the Elements, Oxford: Oxford University Press, s. 3-4
99. J. J. R. Fraústo da Silva, R. J. P. Williams, The Biological Chemistry of the Elements, s. 5
